通化东宝:痛风一类新药THDBH151片申报临床获得受理
通化东宝药业股份有限公司(以下简称“公司”、“通化东宝”)全资子公司东宝紫星(杭州)生物医药有限公司(以下简称“东宝紫星”)于近日取得国家药品监督管理局药品审评中心(CDE)签发的关于THDBH151片临床试验申请受理通知书,受理号为CXHL2200713国、CXHL2200714国、CXHL2200715国。
THDBH151片是一款XO/Urat1双靶点抑制剂用于治疗痛风的药物,同时也是通化东宝在研两款治疗痛风和高尿酸血症的一类创新药之一,另一款URAT1抑制剂(THDBH130片)已于去年成功进入临床试验阶段。THDBH151片申报临床获得受理彰显出公司在向创新药企转型道路上阔步前行的决心和能力。
中国高尿酸血症和痛风患者对高效安全的抗痛风药物仍有迫切的需求,根据《中国高尿酸血症与痛风诊疗指南(2019)》,市场上现有的治疗痛风药物主要包括抑制尿酸生成的以XO为主要靶点的黄嘌呤氧化酶抑制剂(别嘌醇、非布司他)和抑制尿酸重吸收的Urat1抑制剂(苯溴马隆、雷西那德)。这两类药物在有效性和安全性上都有可以改进的空间。以雷西那德为代表的新型Urat1抑制剂是近年来高尿酸血症领域的研究热点,但是临床研究中发现Urat1抑制剂存在急性肾毒性问题。因此Urat1抑制剂需要与XO抑制剂联用,从源头上减少尿酸的生产,以减少急性肾毒性的发生。
公司THDBH151片因其在机制上的特殊优势,既能抑制黄嘌呤氧化酶(XO),从源头上减少尿酸产生,也可抑制肾小管URAT1转运体对尿酸重吸收,加快尿酸排出。此外,THDBH151片通过平衡好XO/Urat1在降尿酸中的作用,在提高药效的同时降低副作用,大幅提高患者依从性,有望成为同领域中Best-in-Class药物。目前国内外均暂无同类产品上市。
近年来,中国高尿酸血症及痛风患者呈明显上升和年轻化趋势。据《中国高尿酸血症与痛风诊疗指南(2019)》及国家统计局第六次人口普查数据显示,中国高尿酸血症的总体患病率为13.3%,患病人数约为1.77亿,痛风总体发病率为1.1%,患病人数约为1,466万。高尿酸血症已成为继糖尿病、高血压、高血脂症后的“第四高”,痛风也已成为仅次于糖尿病的第二大代谢类疾病。
中国痛风和高尿酸血症治疗药物市场空间广阔。根据弗若斯特沙利文分析,未来中国高尿酸血症和痛风患病人数会持续增加,高尿酸血症患病人数预计在2025年/2030年将分别达到2.05亿人/2.39亿人;痛风患病人数预计在2025年/2030年将分别达到4,540万人/5,220万人;对应的中国痛风药物市场规模预计在2025年/2030年将分别增长至29亿元/108亿元。
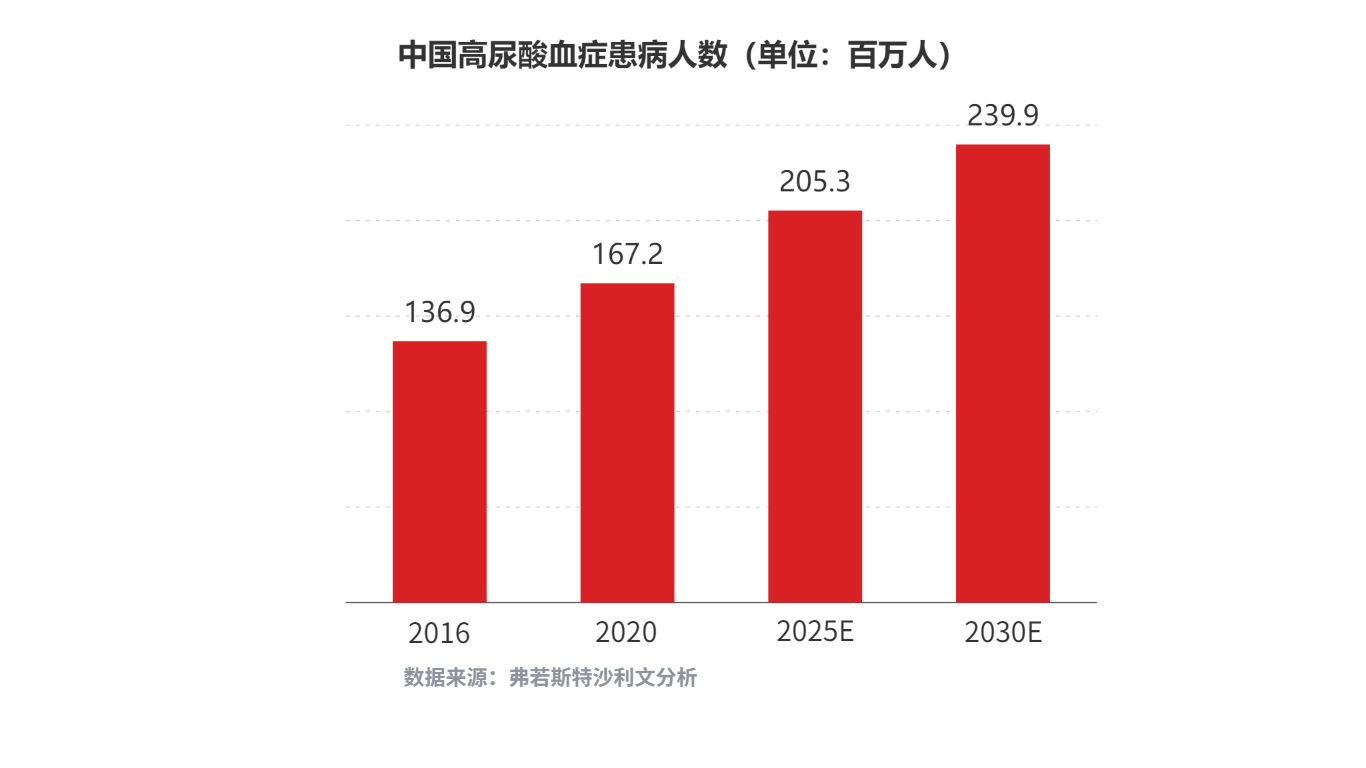
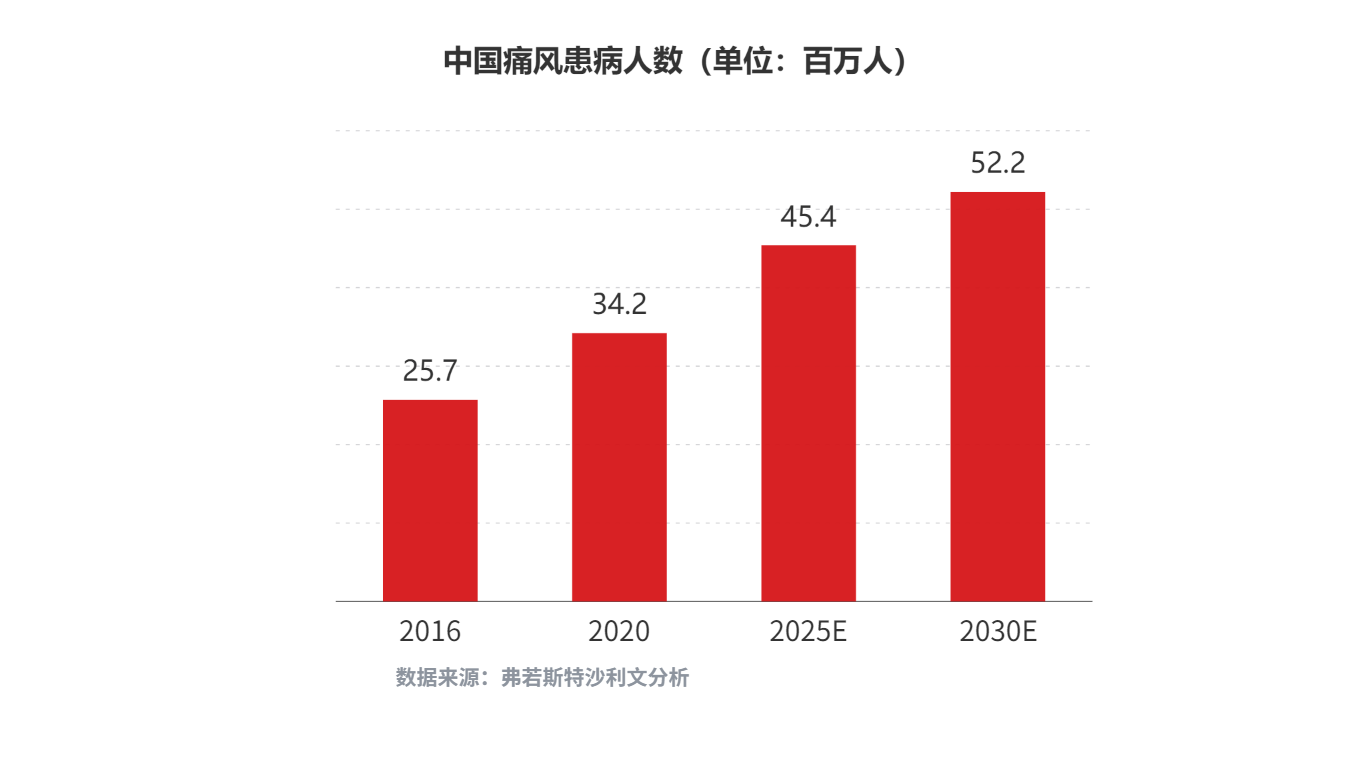
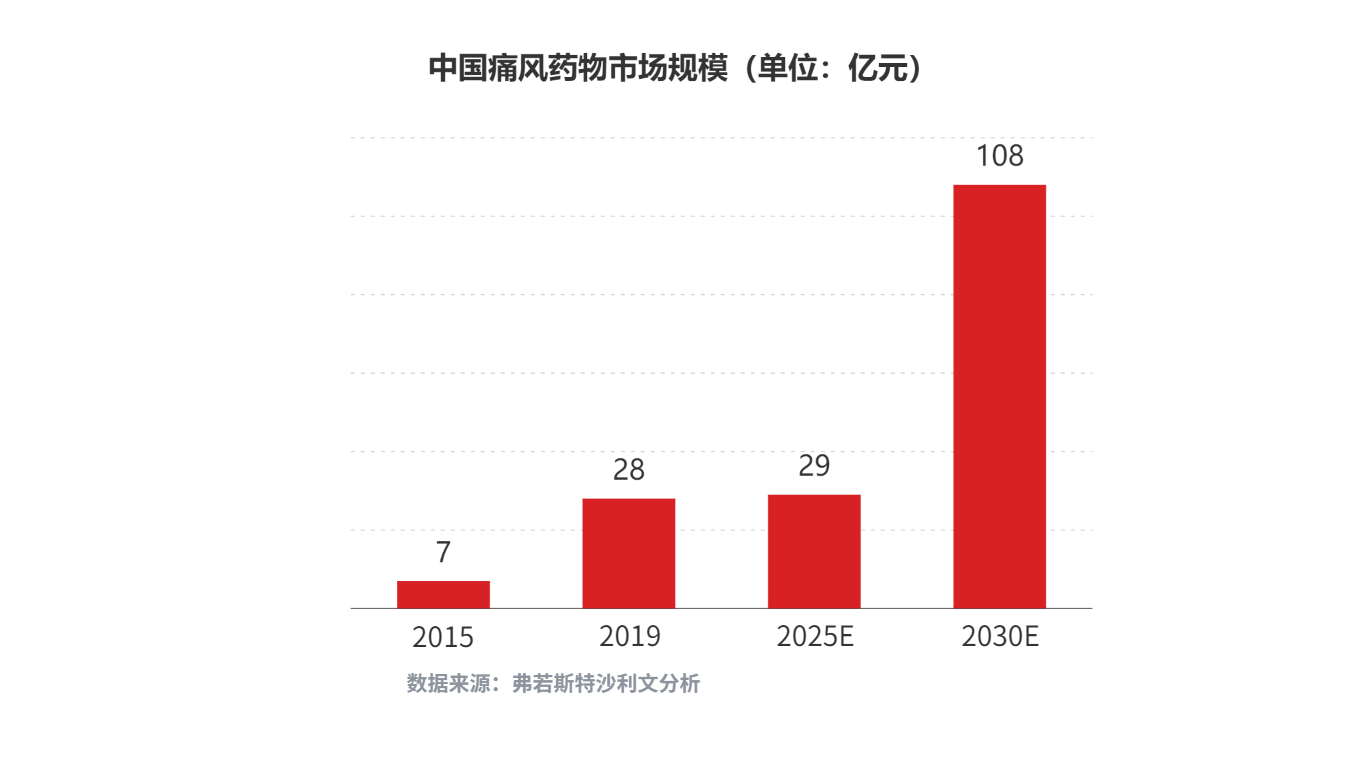
公司THDBH151片申报临床获得受理体现出公司在糖尿病领域外其他内分泌代谢领域的积极进展。未来公司将继续加速推进在痛风和高尿酸血症治疗领域的研发进程,通过自主研发疗效显著且安全性高的创新药物来开拓公司的发展边界,打造新的增长引擎,并与公司现有业务形成协同效应,构筑新的发展空间。









